Elektroneutralität: Stoffe, die aus Ionen aufgebaut sind, sind elektrisch
neutral, das heißt es müssen gleich viel
positive wie negative Ladungen.
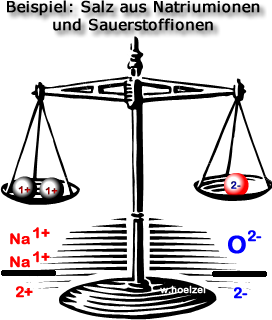
Beispiel: Betrachten wir ein Stoff der aus folgende
Ionen aufgebaut ist: Na1+ und O2-.
Die Ladung dürfen wir nicht so einfach verändern, da
die Edelgasregel erfüllt werden soll. O1- oder Na2+
sind somit falsch.
Wir können also nur die Anzahl der Ionen verändern.
Dabei nimmt man das kleinste gemeinsame Vielfache.
Die Gesamtladung muss 0 ergeben. Folglich brauchen
wir 2 Na1+ und
1 O2- um einen neutralen Stoff zu erhalten.
Lösung:
Natriumoxid = 2 Na1+ + 1 O2-
Verhältnisformel= Na2O1.
Da Chemiker von Natur aus faul sind ( ;-) ), schreiben
sie nie die 1.
Name: Natriumoxid (Dinatriumoxid,
Natriummonooxid)
Ionenschreibweise: 2 Na1+ + O2-
Verhältnisformel: Na2O
Achtung:
Es kommt darauf an, dass gleich
viele Ladungen vorhanden sind;
nicht gleich viele Teilchen!!