Überlegt euch anhand der zwei Bedingungen (polar und asymmetrische Ladungsverteilung), ob ein permanenter
Dipol vorliegt.
Überprüfung: Liegt ein permanenter Dipol vor?
1. Schritt: Besitzt das Molekül eine polare Bindung? Ja!
- Bindung O=C ΔEN = EN(O) - EN(C)
= 3,5 - 2,5 = 1 (polare Bindung liegt vor da zwischen 0,4 und 1,7)
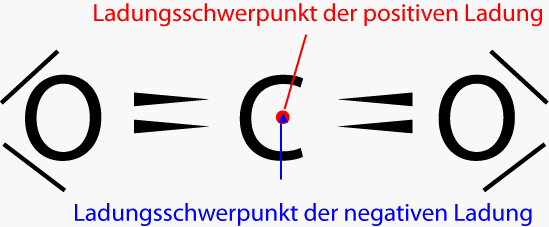
2. Schritt: Fallen die Ladungsschwerpunkte in einem Punkt zusammen (Elektronen sind symmetrisch verteilt)? Ja
Ergebnis: Es liegt kein permanenter Dipol vor. Zwar liegt eine polare Bindung vor, aber die Ladungsschwerpunkte
sind symmetrisch verteilt und somit fallen die Ladungsschwerpunkte in einem Punkt zusammen.