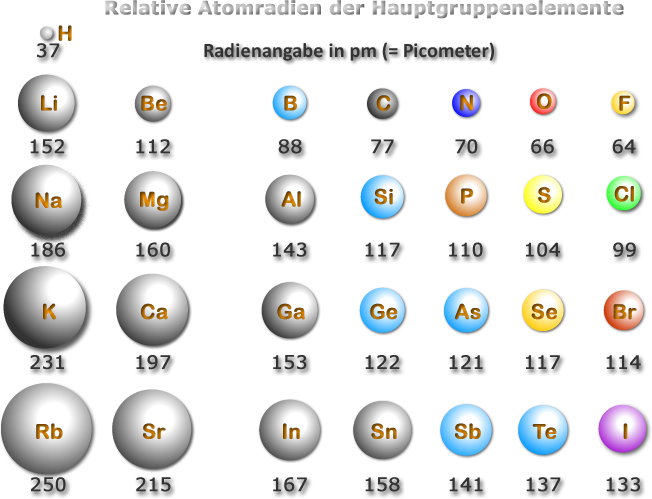
Hier sind die relativen Atomradien der Elemente der Hauptgruppe angegeben, wie sie aus den Bindungslängen
ermittelt wurden. Die Anordnung entspricht der Anordnung innerhalb des PSE.
Überlege dir mögliche Ursachen, warum innerhalb einer Periode (Reihe) die Größe abnimmt und innerhalb einer
Hauptgruppe die Radien zunehmen! Eine mögliche Erklärung findest Du, wenn auf den Lösungsbutton drückst.
Abnahme innerhalb der Periode:
Von rechts nach links nimmt die
Anzahl der Protonen zu. Diese
Protonen ziehen stärker an den
Elektronen: Atomradius wird kleiner.
Zunahme innerhalb der Hauptgruppe:
Von oben nach unten nimmt die
Schalenanzahl (Energieniveaus). Damit ergibt
sich ein größerer Radius.